Riesgo de cáncer de mama (si recibe THS)
Traducido del inglés. Mostrar original.
Last reviewed dd mmm yyyy. Last edited dd mmm yyyy
Para ayudar a la claridad, las publicaciones recientes de este artículo se discuten en contexto con estudios clínicos clave anteriores a ellas, que han influido en la prescripción de THS en el Reino Unido. Se trata del reanálisis del CGHFBC de 1997 de 51 estudios observacionales mundiales, publicaciones previas del estudio aleatorizado WHI, el estudio observacional Million Women's Study (MWS) y la Guía para la Menopausia del National Institute for Health and Care and Excellence del Reino Unido de 2015 (NG23).
- El CGHFBC de 1997 estableció una asociación dependiente de la duración de la THS con el riesgo de diagnóstico, emergente tras 5 años de exposición (un cociente de riesgos global de 1,35). Este riesgo era mayor con la THS combinada que con la THS sin oposición y disminuía tras el cese (1).
- En 2002 y 2004, los resultados iniciales del estudio aleatorizado controlado con placebo WHI confirmaron un aumento global del riesgo de significación limítrofe con la THS combinada continua (es decir, 0,625 mg de estrógenos equinos conjugados [CEE] más 2,5 mg de acetato de medroxiprogesterona [MPA]) (2) (3).
- En 2003, el MWS observacional informó de que el riesgo de cáncer de mama aumentaba con todos los regímenes de THS, y que el mayor aumento del riesgo se asociaba a los preparados combinados. En contraste con todos los demás estudios, el impacto de la THS se observó con el riesgo de uso a corto plazo (es decir, de 6 meses a menos de 2 años). Este hallazgo erróneo se ha atribuido ahora a un sesgo de determinación y a una subestimación de la duración de la exposición a la THS, pero la publicidad adversa que generaron los resultados provocó un descenso significativo de la prescripción de THS en todo el mundo. (4)
Tanto en el estudio WHI como en el MWS, los investigadores hicieron hincapié en el uso de cocientes de riesgo y cambios porcentuales en el riesgo, que fueron malinterpretados. Esto podría haberse evitado presentando los hallazgos utilizando cifras absolutas con encuadre. (5)
- El NG239 de 2015 incluyó una evaluación de los resultados a corto plazo de la THS, con uso de hasta 5 años en los resultados de cáncer de mama. Los estudios clínicos elegibles para revisión fueron en su mayoría observacionales y variaron de calidad baja a moderada en el mejor de los casos y, en general, los hallazgos no difirieron significativamente de los de la evidencia previa. (6)
En consecuencia, las pruebas clínicas anteriores a publicaciones más recientes llevaron a las siguientes conclusiones: (2,3,4)
- La THS con estrógenos solos (CEE, estradiol, estriol) se asoció con ningún o escaso cambio en el riesgo y puede no aumentar con dosis bajas de estrógenos vaginales.
- La THS combinada, administrada por cualquier vía de administración, puede asociarse a un aumento del riesgo, que parece depender de la duración.
- El riesgo de diagnóstico no fue elevado en usuarias anteriores de THS
- El riesgo se limitó a las mujeres delgadas (es decir, sin sobrepeso ni obesidad).
- No parece haber un efecto de la dosis de estrógenos.
- Es posible que no haya habido un efecto aditivo en mujeres con riesgo personal elevado debido a antecedentes familiares o afección mamaria benigna de alto riesgo.
En agosto de 2019, el Collaborative Group on Hormonal Factors in Breast Cancer (CGHFBC) publicó un metaanálisis de más de 100 000 mujeres diagnosticadas de cáncer de mama en relación con el tipo y el momento de la hormonoterapia menopáusica y el riesgo de cáncer de mama (7). Esto también permitió la estimación de los riesgos relativos de cáncer de mama asociados con diferentes duraciones de exposición a, y formulaciones de, terapia hormonal menopáusica (THM) junto con un algoritmo de modelización del cáncer de mama basado en grados de antecedentes familiares.
En 2020 se publicó el informe de resultados a largo plazo del estudio aleatorizado y controlado con placebo Women's Health Initiative (WHI). (8)
En base a esto, la evidencia actual es ahora que (7,8):
1. En mujeres con un riesgo subyacente bajo de cáncer de mama (es decir, la mayoría de la población), los beneficios de la THS durante un uso de hasta 5 años para el alivio de los síntomas superarán los daños potenciales:
- Los estrógenos sin oposición se asocian a un riesgo nulo o muy bajo, pero esto puede estar influido por la edad de inicio.
- No hay pruebas de un efecto de la dosis con los estrógenos.
- Los estrógenos vaginales no se asocian a un aumento del riesgo.
- La THS combinada puede asociarse a un aumento del riesgo, que parece depender de la duración.
- Aunque el riesgo con la THS combinada continua puede ser mayor que con la THS secuencial, la diferencia en el riesgo es pequeña y puede verse compensada por la protección frente al cáncer de endometrio.
- Evitar los progestágenos sintéticos en los preparados combinados puede minimizar el riesgo.
- El riesgo se limita a las mujeres delgadas
- El riesgo asociado a la THS (incluidas las usuarias anteriores) es menor que otros factores de riesgo de cáncer de mama relacionados con el estilo de vida.
- En las mujeres con insuficiencia ovárica prematura, los años de exposición a la THS deben contarse a partir de los 50 años.
- Comunicar el riesgo en términos de exceso de riesgo absoluto con encuadre, minimiza las interpretaciones erróneas.
2. En mujeres de alto riesgo o supervivientes de cáncer de mama (7,8):
- No hay efecto aditivo de la exposición a la THS en mujeres con riesgo personal elevado debido a antecedentes familiares o afección mamaria benigna de alto riesgo.
- Si se considera el uso de THS o de estrógenos vaginales, sólo debe hacerse para el tratamiento de los síntomas de deficiencia estrogénica, previa consulta con el equipo de especialistas en mama de la mujer.
- El estrógeno vaginal puede utilizarse en mujeres que toman tamoxifeno pero no inhibidores de la aromatasa.
El informe del Collaborative Group on Hormonal Factors in Breast Cancer (CGHFBC) también mostró diferencias en los datos relativos a los tumores con receptores de estrógenos positivos y negativos y a la indicación de THM (7):
- entre las usuarias actuales, estos riesgos excesivos de cáncer de mama fueron definitivos incluso durante los años 1-4 (RR de estrógeno-progestágeno 1,60; IC 95%: 1,52-1,69; RR de sólo estrógeno 1,17; 1,10-1,26), y fueron dos veces mayores durante los años 5-14 (RR de estrógeno-progestágeno 2,08; 2,02-2,15; RR de sólo estrógeno 1,33; 1,28-1,37)
- los riesgos de los estrógenos-progestágenos durante los años 5-14 fueron mayores con el uso diario que con el uso menos frecuente de progestágenos (RR 2,30; 2,21-2,40 frente a 1,93; 1,84-2,01; heterogeneidad p<0,0001)
- para un preparado determinado, los RR durante los años 5-14 de uso actual fueron mucho mayores para los tumores con receptores de estrógenos positivos que para los tumores con receptores de estrógenos negativos, fueron similares para las mujeres que empezaron la THM a los 40-44, 45-49, 50-54 y 55-59 años de edad, y se atenuaron al empezar después de los 60 años o por la adiposidad (con poco riesgo de THM con estrógenos solos en mujeres obesas)
- tras dejar la THM, persistía cierto exceso de riesgo durante más de 10 años; su magnitud dependía de la duración del uso previo, con poco exceso tras menos de 1 año de uso de THM
En 2019 la MHRA declaró (9):
En el Reino Unido alrededor de 1 de cada 16 mujeres que nunca usan THS son diagnosticadas con cáncer de mama entre las edades de 50 y 69 años. Esto equivale a 63 casos de cáncer de mama por cada 1000 mujeres. Durante el mismo periodo (edades entre 50 y 69 años), con 5 años de uso de THS, el estudio estimó
- unos 5 casos adicionales de cáncer de mama por cada 1.000 mujeres que utilizan THS con estrógenos solos
- unos 14 casos adicionales de cáncer de mama por cada 1.000 mujeres que utilizaban estrógenos combinados con progestágenos durante parte de cada mes (THS secuencial)
- unos 20 casos más de cáncer de mama por cada 1.000 mujeres que utilizan THS combinada con estrógenos y progestágenos a diario (THS continua).
Estos riesgos se refieren a 5 años de uso de THS. El número de casos adicionales de cáncer de mama mencionado anteriormente se duplicaría aproximadamente si la THS se utilizara durante 10 años en lugar de 5.
La MHRA también declaró (9):
- Todas las formas de THS sistémica están asociadas con un exceso significativo de incidencia de cáncer de mama, independientemente del tipo de estrógeno o progestágeno o de la vía de administración (oral o transdérmica).
- El riesgo aumenta poco o nada con el uso actual o previo de THS durante menos de 1 año; sin embargo, el riesgo aumenta con el uso de THS durante más de 1 año.
- El riesgo de cáncer de mama aumenta aún más con el uso prolongado de THS.
- El riesgo de cáncer de mama es menor tras la interrupción de la THS que durante el uso actual, pero sigue aumentando en las ex usuarias de THS durante más de 10 años en comparación con las mujeres que nunca han utilizado THS.
- El riesgo de cáncer de mama es mayor con la THS combinada de estrógenos y progestágenos que con la THS de estrógenos solos.
- Para las mujeres que utilizan THS durante periodos similares, el número total de cánceres de mama relacionados con la THS a los 69 años es similar si la THS se inicia a los 40 o a los 50 años.
- El estudio no encontró pruebas de un efecto sobre el riesgo de cáncer de mama con el uso de dosis bajas de estrógeno aplicadas directamente por vía vaginal para tratar síntomas locales.
La MHRA ha resumido los riesgos de la THS con respecto al cáncer de mama, de endometrio y de ovario (9):
Summary of HRT risks and benefits* during current use and current use plus post-treatment from age of menopause up to age 69 years, per 1000 women with 5 years or 10 years use of HRT (9)
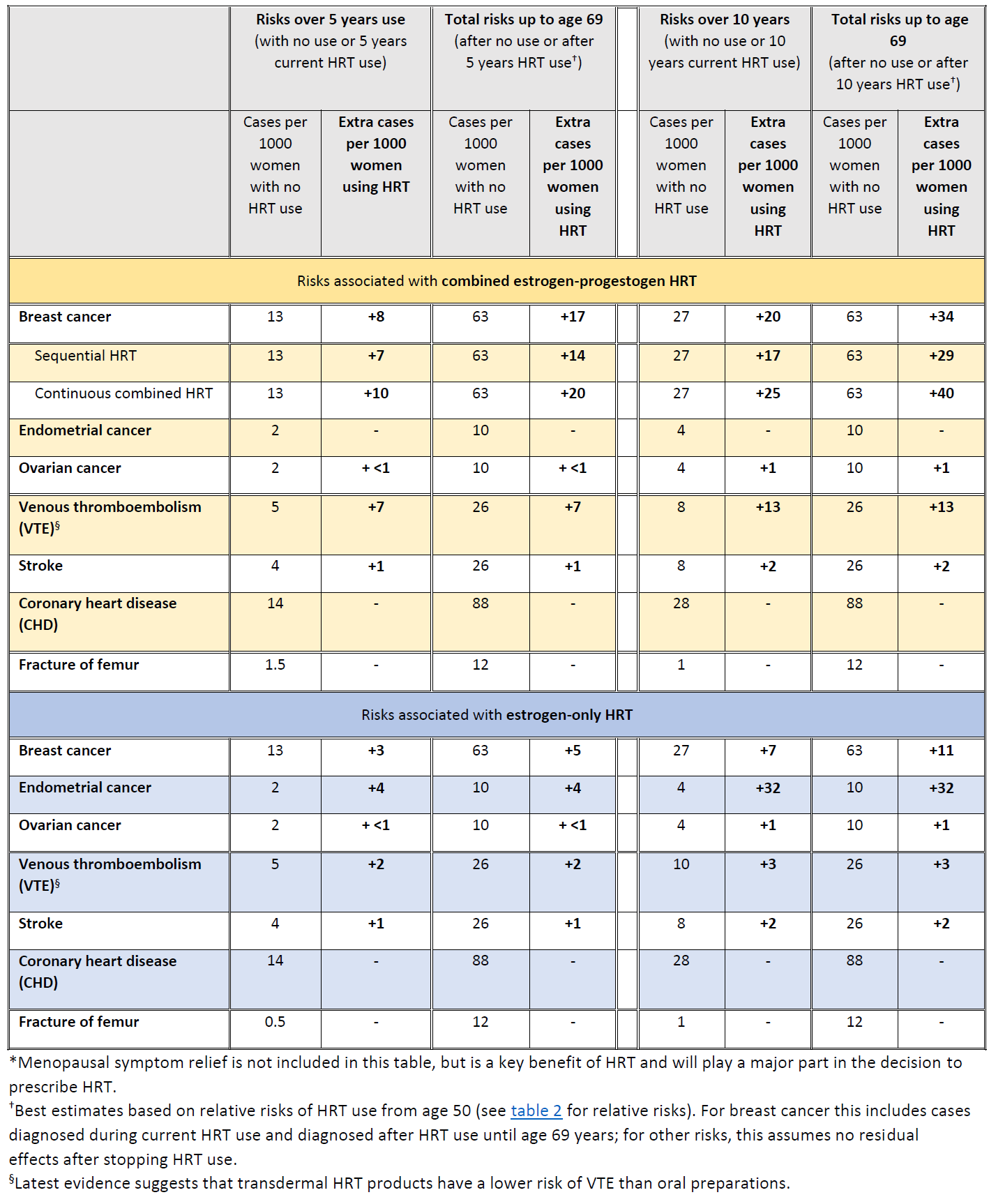
En 2020 se realizó un estudio de 98.611 mujeres de 50 a 79 años con diagnóstico primario de cáncer de mama entre 1998 y 2018, emparejadas por edad, práctica general y fecha índice con 457.498 mujeres control (10). Encontró que el uso anterior a largo plazo de terapia de solo estrógeno y el uso anterior a corto plazo (<5 años) de estrógeno-progestágeno no se asociaron con un mayor riesgo
Una alerta del NIHR relacionada con este estudio afirma que (10):
- La mayoría de las mujeres tomaron THS combinada, lo que se relacionó con un pequeño aumento del riesgo de cáncer de mama. El riesgo aumentó con:
- la edad de la mujer, con un menor aumento del riesgo en las mujeres de 50 años, en comparación con las de 60 y 70 años
- la duración del tratamiento, con un menor aumento del riesgo con la THS tomada a corto plazo (menos de 5 años) que a largo plazo (más de 5 años)
- el tratamiento actual o más reciente con THS, que conlleva mayores riesgos que el uso anterior (hace más de 5 años)
- el tipo de progestágeno de la THS combinada; los mayores riesgos se dieron con la noretisterona y los menores con la didrogesterona.
- Los investigadores subrayaron que algunas mujeres que nunca habían tomado THS seguirían padeciendo cáncer de mama. Por ejemplo, si un grupo de 10.000 mujeres de 50 años nunca hubiera tomado THS, 26 mujeres seguirían padeciendo cáncer de mama en un año. Si las 10.000 mujeres hubieran tomado recientemente THS combinada durante menos de 5 años, 35 padecerían cáncer de mama. Así pues, en este gran grupo de mujeres, la THS está relacionada con 9 casos adicionales de cáncer de mama en un año. Es decir, menos de una de cada mil mujeres.
- El aumento del riesgo estaba relacionado principalmente con la THS combinada, y el tipo de progestágeno marcaba la diferencia. El riesgo aumentaba de forma similar cuando los preparados que contenían algunos tipos de progestágeno (noretisterona, levonorgestrel o medroxiprogesterona) se tomaban durante más de un año. El menor aumento del riesgo se produjo con la dydrogesterona (otro tipo de progestágeno).
- Incluso si las mujeres tomaban THS combinada a largo plazo (más de 5 años), los riesgos se reducían tras interrumpir la terapia. En las mujeres de 50 años, no hubo riesgo adicional de cáncer de mama con la THS combinada interrumpida más de 5 años antes. Hubo poco riesgo adicional entre las mujeres de 60 y 70 años.
- No se observó un aumento del riesgo de cáncer de mama
- con cualquier THS actual tomada durante un año o menos
- con el uso anterior de THS de estrógenos solos, incluso si se tomaba a largo plazo
- con el uso anterior de THS combinada tomada a corto plazo
Riesgo de cáncer de mama si hay antecedentes familiares de cáncer de mama (11)
- Un estudio de modelización realizado en el Reino Unido en 2024 reveló que para una mujer con antecedentes familiares "medios" que no toma THM, el riesgo acumulado de cáncer de mama (edad 50-80 años) es del 9,8%, y el riesgo de muerte por cáncer de mama es del 1,7%.
- en este modelo, se calculó que 5 años de exposición a MHT combinada-cíclica (edad 50-55 años) aumentaba estos riesgos al 11,0% y al 1,8%, respectivamente.
- para una mujer con antecedentes familiares "fuertes" que no toma MHT, el riesgo acumulado de cáncer de mama es del 19,6% (edad 50-80 años), y el riesgo de muerte por cáncer de mama es del 3,2%. Con 5 años de exposición a MHT (edad 50-55 años), este modelo mostró que estos riesgos aumentan al 22,4% y al 3,5%, respectivamente. (11)
- por ejemplo, para una mujer "media" de 51 años que tome THS combinada durante 5 años, la probabilidad de desarrollar un cáncer de mama atribuible a la THS es de 1 en 67
- en el caso de las personas con antecedentes familiares importantes, la probabilidad respectiva es de 1 en 30
- los autores concluyen que, aunque las personas con antecedentes familiares significativos ("importantes") de cáncer de mama tienen un riesgo basal considerablemente mayor de desarrollar cáncer de mama, la mayor parte de la incidencia y mortalidad por cáncer de mama de este grupo se atribuirá a su riesgo basal y no a la adición de THS a los 50 años.
- por ejemplo, para una mujer "media" de 51 años que tome THS combinada durante 5 años, la probabilidad de desarrollar un cáncer de mama atribuible a la THS es de 1 en 67
Nota:
Cualquier riesgo de cáncer de mama debe considerarse en el contexto de los beneficios y riesgos generales asociados a la toma de hormonoterapia menopáusica (THM), incluyendo el control de los síntomas menopáusicos, la mejora de la calidad de vida y el impacto a largo plazo sobre la salud ósea y cardiovascular. La decisión de tomar o no THM, la dosis de THM y la duración de su uso deben tomarse de forma individualizada tras discutir los beneficios y riesgos con las mujeres para ayudarlas a tomar una decisión informada sobre su salud y cuidados.
Referencia:
- Grupo Colaborador sobre Factores Hormonales para el Cáncer de Mama. Cáncer de mama y terapia hormonal sustitutiva: Reanálisis colaborativo de 51 estudios epidemiológicos individuales. Lancet 1997; 350: 1047-1060
- Grupo de redacción de los investigadores de la Women's Health Initiative. Riesgos y beneficios del estrógeno más progestina en mujeres posmenopáusicas sanas. JAMA 2002; 288: 321- 333
- Anderson GL, Limacher M, Assaf AR et al; Womens's Health Initiative Steering Committee. Effects of conjugated equine estrogen in postmenopausal women with hysterectomy: The Women's Health Initiative randomized controlled trial. JAMA, 2004; 291: 1701-12
- Colaboradores del estudio Million Women. Cáncer de mama y terapia hormonal sustitutiva en el Million Women Study. Lancet 2003; 362: 419-427
- Gigerenzer G. How innumeracy can be exploited, en Reckoning with Risk, editorial Penguin Group, 2003.
- National Institute for Health and Care Excellence; Menopause; Clinical Guideline - methods, evidence and recommendations (NG23), 2015 www.nice.org.uk/guidance/ ng23
- Grupo de colaboración sobre factores hormonales para el cáncer de mama. Type and timing of menopausal hormone therapy and breast cancer risk: individual participant meta-analysis of the worldwide epidemiological evidence, doi.org/10.1016/S0140- 6736(19)31709-X
- Chlebowski RT, Anderson GL, Aragaki AK et al. Association of menopausal hormone replacement therapy with breast cancer incidence and mortality during long-term follow-up of the Women's Health Initiative randomised clinical trials. JAMA, 2020; 324: 369-380.
- MHRA (agosto de 2019). Terapia hormonal sustitutiva y riesgo de cáncer de mama.
- Vinogradova Y, Coupland C, Hippisley-Cox J. Uso de terapia de reemplazo hormonal y riesgo de cáncer de mama: estudios de casos y controles anidados utilizando las bases de datos QResearch y CPRD. BMJ 2020;371:m3873.
- Huntley C et al. Evaluación del riesgo de cáncer de mama para la prescripción de terapia hormonal menopáusica en mujeres con antecedentes familiares de cáncer de mama. British Journal of General Practice 9 mayo 2024
Páginas relacionadas
- Terapia hormonal sustitutiva (THS) en pacientes con cáncer de mama
- Cáncer de mama
- Terapia hormonal sustitutiva
- Tibolona
- Cardiopatías y THS
- Riesgo de cáncer si se interrumpe la THS
- Indicaciones clínicas de la THS (terapia hormonal sustitutiva)
- Orientaciones del NICE - THS y riesgo de cáncer de mama
- Revisión de la evidencia sobre el riesgo de cáncer de mama y la THS
Crear una cuenta para añadir anotaciones a la página
Añada a esta página información que sería útil tener a mano durante una consulta, como una dirección web o un número de teléfono. Esta información se mostrará siempre que visite esta página