Bis zu 10 % der Brustkrebsfälle in den westlichen Ländern sind auf eine genetische Veranlagung zurückzuführen. Die Anfälligkeit für Brustkrebs wird offenbar autosomal-dominant mit begrenzter Penetranz vererbt und kann daher entweder vom Vater oder von der Mutter vererbt werden. Etwa 5 % der Brustkrebsfälle sind auf hochpenetrante dominante Gene zurückzuführen.
Es wird angenommen, dass mehr als fünf Gene daran beteiligt sind. Das wichtigste scheint das BRCA1-Gen zu sein, das sich auf Chromosom 17q befindet. Dieses Gen wurde kürzlich kloniert, und es wird vermutet, dass es in verschiedenen Regionen Mutationen aufweist. Zu den anderen identifizierten Genen gehören BRCA2 auf 13q und das p53-Gen auf 17p.
- BRCA1-Trägerinnen haben ein Lebenszeitrisiko von annähernd 80 %, an Brustkrebs zu erkranken, und ein erhöhtes Risiko für Eierstockkrebs (40-60 %) (1)
- BRCA2 birgt ein geringeres Risiko für Eierstockkrebs (20-30 %), ist aber mit einem erhöhten Risiko für ein breiteres Spektrum anderer Krebsarten verbunden, darunter Prostatakrebs, Bauchspeicheldrüsenkrebs und ein erhöhtes Risiko für männlichen Brustkrebs
- In der allgemeinen kaukasischen Bevölkerung des Vereinigten Königreichs liegt die Häufigkeit von Mutationen in BRCA1 oder BRCA2 bei etwa 1/400; in der aschkenasischen Bevölkerung beträgt die Häufigkeit dieser Mutationen etwa 2% (1)
- Die Behandlung von Brustkrebs bei BRCA1- und BRCA2-Trägerinnen ist derzeit dieselbe wie bei sporadischen Fällen, mit der Ausnahme, dass bei der primären Operation eine beidseitige Mastektomie angeboten werden kann, da das Risiko der Entwicklung von Brustkrebs in der kontralateralen Brust erhöht ist (etwa 4 % pro Jahr) (1)
Zu den Merkmalen des familiären Brustkrebses gehören:
- frühes Alter der Erkrankung
- mehrere Verwandte sind betroffen
- bilaterale Beteiligung ist häufig
- Vorgeschichte mit verwandten Krebsarten - Dickdarm, Eierstock, Gebärmutterschleimhaut
Wenn ein Verwandter ersten Grades an Brustkrebs erkrankt ist, beträgt das relative Risiko, an Brustkrebs zu erkranken, 1,7 bis 2,5. Ist eine Verwandte zweiten Grades betroffen, liegt das relative Risiko bei 1,5.
Bei einigen wenigen geeigneten Familien sind DNA-Tests möglich.
Mutationen im CHEK2-Gen können das Brustkrebsrisiko um das Zweifache erhöhen (1).
Mutationen im TP53-Gen erhöhen das Risiko für ein breites Spektrum von Tumoren, darunter Sarkome, Nebennierenrindenkarzinome, Hirntumore und sehr früh auftretender Brustkrebs.
NICE schlägt vor (4):
- Trägerwahrscheinlichkeit, bei der ein Gentest angeboten werden sollte
- Wenn in der Sekundärversorgung verfügbar, verwenden Sie eine Berechnungsmethode für die Trägerwahrscheinlichkeit mit nachgewiesener akzeptabler Leistung (in Bezug auf Kalibrierung und Diskriminierung) sowie die Familienanamnese, um zu bestimmen, wem eine Überweisung an eine genetische Spezialklinik angeboten werden sollte. Beispiele für akzeptable Methoden sind BOADICEA und das Manchester-Scoring-System
- Angebot von Gentests in genetischen Spezialkliniken für Verwandte mit einer persönlichen Vorgeschichte von Brust- und/oder Eierstockkrebs, wenn diese eine kombinierte BRCA1- und BRCA2-Mutationsträgerwahrscheinlichkeit von 10 % oder mehr aufweisen
- Angebot von Gentests in genetischen Spezialkliniken für Personen ohne persönliche Vorgeschichte von Brust- oder Eierstockkrebs, wenn die kombinierte BRCA1- und BRCA2-Mutationsträgerwahrscheinlichkeit 10 % oder mehr beträgt und ein betroffener Verwandter für den Test nicht zur Verfügung steht.
- Brustkrebs-Risikokategorie
Bevölkerungsnahes Risiko | Mäßiges Risiko | Hohes Risiko * | |
Lebenslanges Risiko ab Alter 20 | Weniger als 17% | Mehr als 17%, aber weniger als 30% | 30% oder mehr |
Risiko zwischen 40 und 50 Jahren | Weniger als 3% | 3-8% | Mehr als 8% |
*Zu dieser Gruppe gehören bekannte BRCA1-, BRCA2- und TP53-Mutationen sowie seltene Erkrankungen, die mit einem erhöhten Brustkrebsrisiko verbunden sind, wie das Peutz-Jegher-Syndrom (STK11), Cowden (PTEN) und familiärer diffuser Magenkrebs (E-Cadherin)
- Überwachung von Frauen ohne Brustkrebs in der Vorgeschichte
- Angebot einer jährlichen mammographischen Überwachung für Frauen:
- im Alter von 40-49 Jahren mit mittlerem Brustkrebsrisiko
- im Alter von 40-59 Jahren mit hohem Brustkrebsrisiko, aber einer Wahrscheinlichkeit von 30 % oder weniger, BRCA- oder TP53-Trägerin zu sein
- Frauen im Alter von 40-59 Jahren, die sich keinem Gentest unterzogen haben, aber mit einer Wahrscheinlichkeit von mehr als 30% BRCA-Trägerinnen sind
- im Alter von 40-69 Jahren mit einer bekannten BRCA1- oder BRCA2-Mutation
- Angebot einer jährlichen MRT-Überwachung für Frauen:
- Frauen im Alter von 30-49 Jahren, die sich keinem Gentest unterzogen haben, aber mit einer Wahrscheinlichkeit von mehr als 30% BRCA-Trägerinnen sind
- im Alter von 30 bis 49 Jahren mit einer bekannten BRCA1- oder BRCA2-Mutation
- im Alter von 20-49 Jahren, die sich keinem Gentest unterzogen haben, aber mit einer Wahrscheinlichkeit von mehr als 30% TP53-Träger sind
- im Alter von 20-49 Jahren mit einer bekannten TP53-Mutation
- Angebot einer jährlichen mammographischen Überwachung für Frauen:
- Überwachung für Frauen mit einer persönlichen und familiären Brustkrebsanamnese
- Angebot einer jährlichen mammographischen Überwachung für alle Frauen im Alter von 50-69 Jahren mit einer persönlichen Vorgeschichte von Brustkrebs, die:
- weiterhin ein hohes Brustkrebsrisiko haben (einschließlich derjenigen, die eine BRCA1- oder BRCA2-Mutation haben) und
- die keine TP53-Mutation haben
- Angebot einer jährlichen MRT-Überwachung für alle Frauen im Alter von 30-49 Jahren mit einer persönlichen Brustkrebsanamnese, die weiterhin ein hohes Brustkrebsrisiko haben, einschließlich derjenigen, die eine BRCA1- oder BRCA2-Mutation aufweisen
- Angebot einer jährlichen mammographischen Überwachung für alle Frauen im Alter von 50-69 Jahren mit einer persönlichen Vorgeschichte von Brustkrebs, die:
- Chemoprävention für Frauen ohne Brustkrebs in der Vorgeschichte
- postmenopausalen Frauen mit Gebärmutter und hohem Brustkrebsrisiko entweder Tamoxifen oder Raloxifen für 5 Jahre anbieten, es sei denn, sie haben eine Vorgeschichte oder ein erhöhtes Risiko für thromboembolische Erkrankungen oder Endometriumkrebs
- postmenopausalen Frauen mit Gebärmutter und hohem Brustkrebsrisiko entweder Tamoxifen oder Raloxifen für 5 Jahre anbieten, es sei denn, sie haben eine Vorgeschichte oder ein erhöhtes Risiko für thromboembolische Erkrankungen oder Endometriumkrebs
- Risikoreduzierte Mastektomie bei Frauen ohne Brustkrebs in der Vorgeschichte
- Alle Frauen, die eine beidseitige risikomindernde Mastektomie in Erwägung ziehen, sollten die Möglichkeit haben, ihre Optionen für eine Brustrekonstruktion (sofort und später) mit einem Mitglied eines chirurgischen Teams zu besprechen, das über spezielle Kenntnisse in Onkoplastik oder Brustrekonstruktion verfügt.
Brustkrebsrisiko bei familiärer Vorbelastung mit Brustkrebs
- Eine britische Modellstudie ergab, dass das kumulative Brustkrebsrisiko für Frauen mit einer "durchschnittlichen" Familienanamnese, die keine HRT einnehmen, bei 9,8 % liegt und sich bei einer kombinierten zyklischen HRT über 5 Jahre auf 11,0 % erhöht. Bei Frauen mit einer ausgeprägten Familienanamnese liegt das Risiko bei 19,6 % (ohne HRT) und erhöht sich auf 22,4 % bei einer 5-jährigen HRT (5)
- Bei einer "durchschnittlichen" 51-Jährigen, die 5 Jahre lang eine kombinierte HRT einnimmt, liegt die Wahrscheinlichkeit, an Brustkrebs zu erkranken, bei 1 zu 67
- bei Personen mit einer ausgeprägten Familienanamnese liegt die entsprechende Wahrscheinlichkeit bei 1:30
- Die Autoren kommen zu dem Schluss, dass, obwohl Personen mit einer signifikanten ("starken") familiären Brustkrebsanamnese ein erheblich erhöhtes Ausgangsrisiko für die Entwicklung von Brustkrebs haben, der größte Teil der Brustkrebsinzidenz und -sterblichkeit für diese Gruppe auf ihr Ausgangsrisiko und nicht auf die zusätzliche HRT im Alter von 50 Jahren zurückzuführen ist.
- Bei einer "durchschnittlichen" 51-Jährigen, die 5 Jahre lang eine kombinierte HRT einnimmt, liegt die Wahrscheinlichkeit, an Brustkrebs zu erkranken, bei 1 zu 67
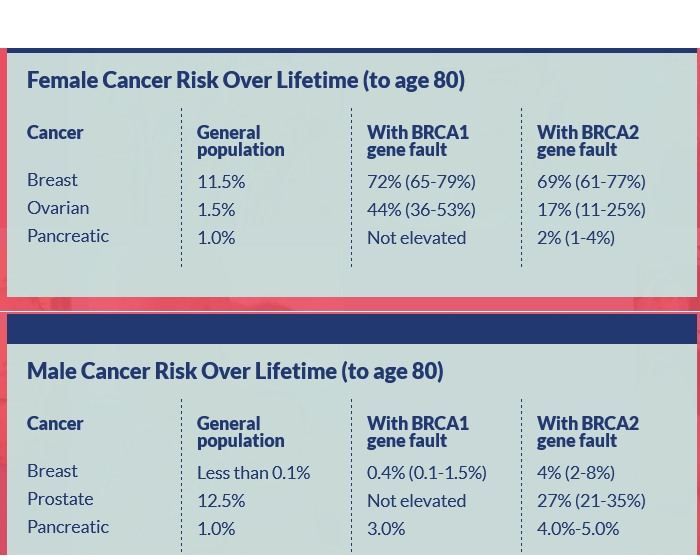
Das NHS Jüdisches BRCA-Testprogramm nennt die verschiedenen Krebsarten, die mit BRCA1 und BRACA2 assoziiert sind:
Referenz:
- Pulse (2005); 65(14):55-60.
- Evans DGR et al. (1994). Familiärer Brustkrebs. BMJ; 308:183-7
- McPherson et al. (1994). BMJ;309:1004
- NICE (June 2013). Familiärer Brustkrebs - Einstufung und Versorgung von Personen mit familiärem Brustkrebsrisiko und Management von Brustkrebs und damit verbundenen Risiken bei Personen mit einer familiären Brustkrebsvorgeschichte
- Huntley C et al. Bewertung des Brustkrebsrisikos für die Verschreibung einer Hormontherapie in den Wechseljahren bei Frauen mit einer familiären Vorgeschichte von Brustkrebs. Britische Zeitschrift für Allgemeinmedizin 9 Mai 2024
Verwandte Seiten
- Brustkrebs
- Prophylaktische Mastektomie bei Patientinnen mit BRCA-Mutationen
- Risiko für Eierstockkrebs in der Familienanamnese
- Überweisungskriterien von der Primärversorgung - bei familiärer Vorbelastung mit Brustkrebs
- TP53-Gen
- Chemoprävention, wenn keine persönliche Vorgeschichte von Brustkrebs vorliegt
- Mastektomie, wenn keine persönliche Vorgeschichte von Brustkrebs vorliegt
- Oophorektomie, wenn in der Vorgeschichte kein Brustkrebs aufgetreten ist
Erstellen Sie ein Konto, um Seitenanmerkungen hinzuzufügen
Fügen Sie dieser Seite Informationen hinzu, die Sie während eines Beratungsgesprächs benötigen, z. B. eine Internetadresse oder eine Telefonnummer. Diese Informationen werden immer angezeigt, wenn Sie diese Seite besuchen