Para maior clareza, as publicações recentes neste artigo são discutidas em contexto com os principais estudos clínicos anteriores a elas, que influenciaram a prescrição de TRH no Reino Unido. Estes foram a reanálise de 1997 do CGHFBC de 51 estudos observacionais a nível mundial, publicações anteriores do estudo aleatório WHI, o estudo observacional Million Women's Study (MWS) e o National Institute for Health and Care and Excellence Menopause Guidance (NG23) de 2015 do Reino Unido
- O CGHFBC de 1997 estabeleceu uma associação dependente da duração da TRH com o risco de diagnóstico, que surgiu após 5 anos de exposição (um rácio de risco global de 1,35). Este parece ser maior com a TRH combinada do que com a TRH sem oposição e diminui após a cessação (1)
- Em 2002 e 2004, os resultados iniciais do estudo WHI, aleatorizado e controlado por placebo, confirmaram um aumento global do risco de significância limítrofe com a TRH combinada contínua (ou seja, 0,625 mg de estrogénio equino conjugado [CEE] mais 2,5 mg de acetato de medroxiprogesterona [MPA] (2) (3)
- Em 2003, o estudo observacional MWS relatou um aumento do risco de cancro da mama com todos os regimes de TRH, sendo o maior aumento do risco associado às preparações combinadas. Em contraste com todos os outros estudos, o impacto da TRH foi observado com o risco de utilização a curto prazo (ou seja, 6 meses a menos de 2 anos). Esta conclusão errónea foi agora atribuída a um viés de apuramento e à subestimação da duração da exposição à TSH, mas a publicidade adversa que os resultados geraram provocou uma queda significativa na prescrição de TSH em todo o mundo. (4)
Tanto no estudo WHI como no MWS, os investigadores colocaram a tónica na utilização de rácios de risco e na alteração percentual do risco, que foram mal interpretados. Este facto poderia ter sido evitado se os resultados fossem apresentados em números absolutos e enquadrados. (5)
- A NG239 de 2015 incluiu uma avaliação dos resultados a curto prazo da TRH, com utilização até 5 anos nos resultados do cancro da mama. Os estudos clínicos elegíveis para revisão eram maioritariamente observacionais e de qualidade baixa a moderada, na melhor das hipóteses, e, de um modo geral, os resultados não diferiram significativamente dos resultados de provas anteriores. (6)
Por conseguinte, as provas clínicas anteriores a publicações mais recentes levaram às seguintes conclusões: (2,3,4)
- A TRH com estrogénio isolado (CEE, estradiol, estriol) foi associada a nenhuma ou pouca alteração no risco e pode não ser aumentada com estrogénio vaginal de baixa dose.
- A TRH combinada, efectuada por qualquer via de administração, pode estar associada a um risco acrescido, que parece depender da duração.
- O risco de diagnóstico não foi elevado em utilizadoras anteriores de TRH
- O risco foi limitado a mulheres magras (ou seja, sem excesso de peso ou obesidade)
- Não parece haver um efeito de dosagem com estrogénio
- Pode não ter havido um efeito aditivo em mulheres com um risco pessoal elevado devido a antecedentes familiares ou a uma doença benigna da mama de alto risco.
Em agosto de 2019, foi publicada pelo Collaborative Group on Hormonal Factors in Breast Cancer (CGHFBC) uma meta-análise de mais de 100 000 mulheres diagnosticadas com cancro da mama em relação ao tipo e ao momento da terapêutica hormonal na menopausa e ao risco de cancro da mama (7). Isto também permitiu estimar os riscos relativos de cancro da mama associados a diferentes durações de exposição e formulações da terapia hormonal da menopausa (MHT), juntamente com um algoritmo de modelação do cancro da mama baseado em graus de história familiar.
Em 2020, foi publicado o relatório de resultados a longo prazo do estudo aleatório e controlado por placebo Women's Health Initiative (WHI). (8)
Com base nisto, a evidência atual é agora a seguinte (7,8):
1. Nas mulheres com um risco subjacente baixo de cancro da mama (ou seja, a maior parte da população), os benefícios da TRH até 5 anos de utilização para alívio dos sintomas excedem os potenciais danos:
- Os estrogénios sem oposição estão associados a nenhuma ou a poucas alterações no risco, mas este pode ser influenciado pela idade de início
- Não há provas de um efeito de dosagem com estrogénios
- O estrogénio vaginal não está associado a um risco acrescido
- A TRH combinada pode estar associada a um risco acrescido, que parece depender da duração
- Embora o risco com a TRH combinada contínua possa ser maior do que com a TRH sequencial, a diferença no risco é pequena e pode ser compensada pela proteção contra o cancro do endométrio
- Evitar o uso de progestagénios sintéticos em preparações combinadas pode minimizar o risco
- O risco é limitado às mulheres magras
- O risco associado à TRH (incluindo utilizadoras anteriores) é menor do que outros factores de risco de cancro da mama associados ao estilo de vida
- Nas mulheres com insuficiência ovárica prematura, os anos de exposição à TSH devem ser contados a partir dos 50 anos de idade
- A comunicação do risco em termos de excesso de risco absoluto com enquadramento minimiza as interpretações erróneas.
2. Em mulheres com risco elevado ou sobreviventes de cancro da mama (7,8):
- Não existe um efeito aditivo da exposição à TRH em mulheres com um risco pessoal elevado devido a antecedentes familiares ou a uma doença benigna da mama de alto risco.
- Se for considerada a utilização de TRH ou de estrogénios vaginais, esta deve ser apenas para o tratamento dos sintomas de deficiência de estrogénios, após discussão com a equipa de especialistas da mama da mulher
- O estrogénio vaginal pode ser utilizado em mulheres que tomam tamoxifeno, mas não inibidores da aromatase.
O relatório do Collaborative Group on Hormonal Factors in Breast Cancer (CGHFBC) também mostrou diferenças nos dados relativos aos tumores com receptores de estrogénio positivos e negativos e à indicação de MHT (7):
- entre as utilizadoras actuais, estes riscos excessivos de cancro da mama eram definitivos mesmo durante os anos 1-4 (estrogénio-progestagénio RR 1,60, 95% CI 1,52-1,69; estrogénio apenas RR 1,17, 1,10-1,26), e eram duas vezes maiores durante os anos 5-14 (estrogénio-progestagénio RR 2,08, 2,02-2,15; estrogénio apenas RR 1,33, 1,28-1,37)
- os riscos de estrogénio-progestagénio durante os anos 5-14 foram maiores com a utilização diária do que com a utilização menos frequente de progestagénio (RR 2,30, 2,21-2,40 vs 1,93, 1,84-2,01; heterogeneidade p<0,0001)
- para uma determinada preparação, os RRs durante os anos 5-14 de utilização atual foram muito maiores para os tumores com receptores de estrogénio positivos do que para os tumores com receptores de estrogénio negativos, foram semelhantes para as mulheres que iniciaram a MHT com idades entre os 40-44, 45-49, 50-54 e 55-59 anos, e foram atenuados pelo início após os 60 anos ou pela adiposidade (com pouco risco de MHT apenas com estrogénio em mulheres obesas)
- após a cessação da MHT, algum excesso de risco persistiu por mais de 10 anos; a sua magnitude dependeu da duração do uso anterior, com pouco excesso após menos de 1 ano de uso de MHT
Em 2019, a MHRA declarou (9):
No Reino Unido, cerca de 1 em cada 16 mulheres que nunca utilizaram TRH são diagnosticadas com cancro da mama entre os 50 e os 69 anos de idade. Isto equivale a 63 casos de cancro da mama por cada 1000 mulheres. Durante o mesmo período (idades 50-69 anos), com 5 anos de utilização de TRH, o estudo estimou
- cerca de 5 casos adicionais de cancro da mama por cada 1000 mulheres que utilizam a TRH apenas com estrogénios
- cerca de 14 casos adicionais de cancro da mama por cada 1000 mulheres que utilizam estrogénio combinado com progestagénio durante parte de cada mês (TRH sequencial)
- cerca de 20 casos adicionais de cancro da mama por cada 1000 mulheres que utilizam a TRH de estrogénio combinada com progestagénio diariamente (TRH contínua)
Estes riscos referem-se a 5 anos de utilização da TRH. O número de casos adicionais de cancro da mama acima referido duplicaria aproximadamente se a TRH fosse utilizada durante 10 anos em vez de 5.
A MHRA também declarou (9):
- Todas as formas de TRH sistémica estão associadas a um excesso significativo de incidência de cancro da mama, independentemente do tipo de estrogénio ou progestagénio ou da via de administração (oral ou transdérmica)
- Há pouco ou nenhum aumento do risco com a utilização atual ou anterior de TRH durante menos de 1 ano; no entanto, há um aumento do risco com a utilização de TRH durante mais de 1 ano
- O risco de cancro da mama aumenta ainda mais com uma duração mais longa da utilização da TRH
- O risco de cancro da mama é menor após a interrupção da TRH do que durante a utilização atual, mas permanece aumentado em ex-utilizadoras de TRH durante mais de 10 anos, em comparação com mulheres que nunca utilizaram TRH
- O risco de cancro da mama é mais elevado com a TRH combinada de estrogénio-progestagénio do que com a TRH apenas de estrogénio
- Para as mulheres que utilizam a TRH durante períodos de tempo semelhantes, o número total de cancros da mama relacionados com a TRH aos 69 anos é semelhante, quer a TRH tenha sido iniciada aos 40 ou aos 50 anos
- O estudo não encontrou provas de um efeito no risco de cancro da mama com a utilização de doses baixas de estrogénio aplicadas diretamente através da vagina para tratar sintomas locais
A MHRA resumiu os riscos da TRH no que diz respeito ao cancro da mama, do endométrio e do ovário (9):
Resumo dos riscos e benefícios da TRH* durante a utilização atual e a utilização atual mais pós-tratamento desde a idade da menopausa até aos 69 anos, por 1000 mulheres com 5 anos ou 10 anos de utilização de TRH (9)
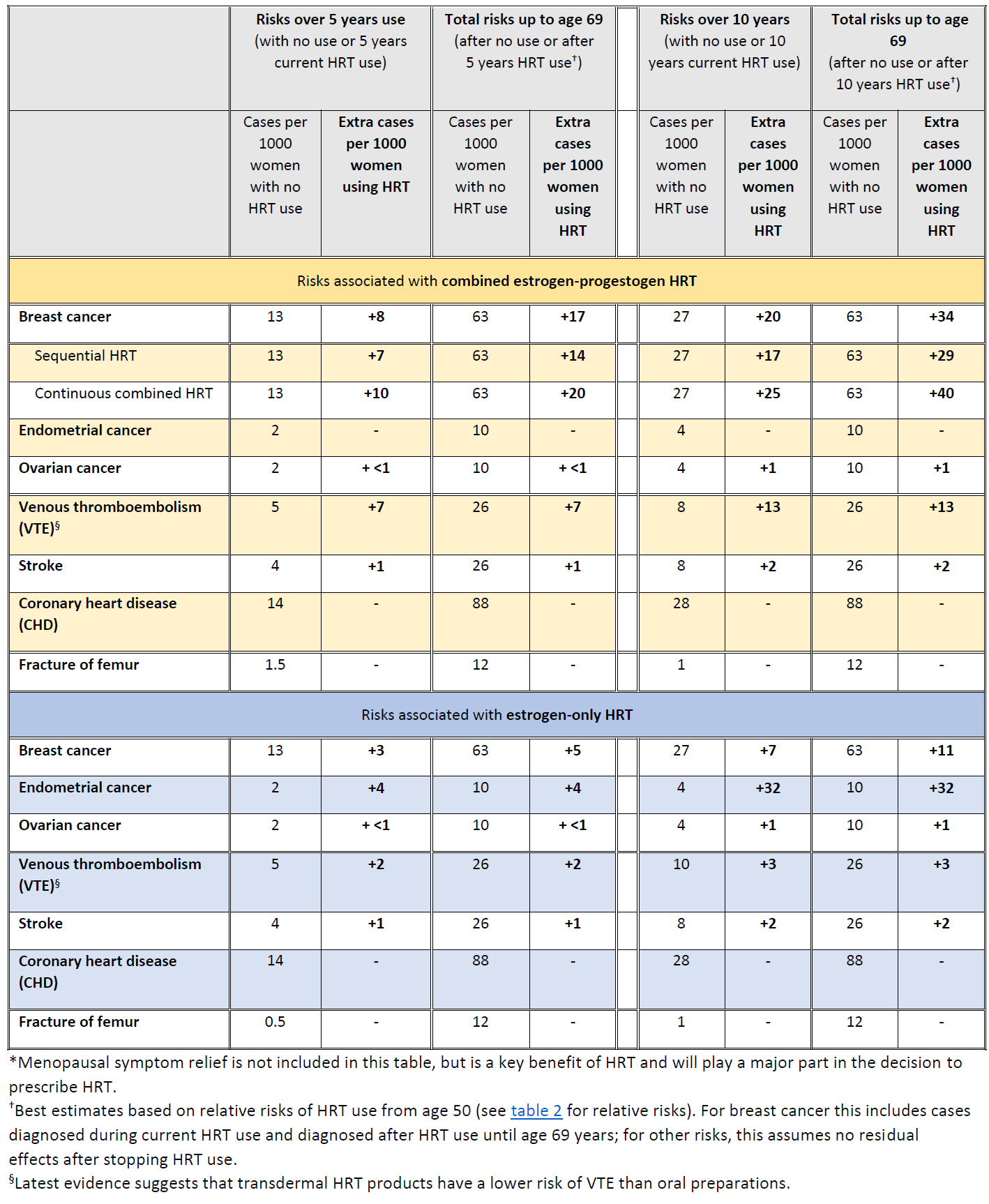
Em 2020, foi realizado um estudo de 98 611 mulheres com idades compreendidas entre os 50 e os 79 anos com um diagnóstico primário de cancro da mama entre 1998 e 2018, emparelhadas por idade, prática geral e data de índice com 457 498 mulheres de controlo (10). Verificou-se que a utilização anterior a longo prazo de terapia apenas com estrogénio e a utilização anterior a curto prazo (<5 anos) de estrogénio-progestagénio não foram associadas a um risco acrescido
Um alerta do NIHR relacionado com este estudo refere que (10):
- A maioria das mulheres tomou TRH combinada, que foi associada a um pequeno aumento do risco de cancro da mama. O risco aumentou com:
- a idade da mulher, com um menor aumento do risco para as mulheres na casa dos 50 anos, em comparação com as mulheres na casa dos 60 e 70 anos
- a duração do tratamento, com menores aumentos do risco com a TRH tomada a curto prazo (menos de 5 anos) do que a longo prazo (mais de 5 anos)
- o tratamento atual ou mais recente da TRH, que apresenta riscos mais elevados do que a utilização anterior (há mais de 5 anos)
- o tipo de progestagénio na TRH combinada; os riscos mais elevados são os da noretisterona e os mais baixos os da didrogesterona.
- Os investigadores sublinharam que algumas mulheres que nunca tomaram TRH continuariam a ter cancro da mama. Por exemplo, se um grupo de 10 000 mulheres na casa dos 50 anos nunca tivesse tomado TRH, 26 mulheres teriam cancro da mama num ano. Se todas as 10 000 mulheres tivessem tomado recentemente TRH combinada durante menos de 5 anos, 35 teriam cancro da mama. Assim, neste grande grupo de mulheres, a TRH está associada a 9 casos extra de cancro da mama num ano. Ou seja, menos de um em cada mil mulheres.
- O risco acrescido estava sobretudo associado à TRH combinada, e o tipo de progestagénio fazia a diferença. O risco aumentou de forma semelhante quando as preparações contendo alguns tipos de progestagénio (noretisterona, levonorgestrel ou medroxiprogesterona) foram tomadas durante mais de um ano. O menor aumento do risco verificou-se com a didrogesterona (outro tipo de progestagénio).
- Mesmo quando as mulheres tomam TRH combinada a longo prazo (mais de 5 anos), os riscos diminuem após a interrupção da terapêutica. Para as mulheres na casa dos 50 anos, não houve risco adicional de cancro da mama com a TRH combinada que foi interrompida há mais de 5 anos. Nas mulheres com 60 e 70 anos, o risco adicional foi reduzido.
- Não se verificou um aumento do risco de cancro da mama:
- com qualquer TRH atual tomada durante um ano ou menos
- com a utilização anterior de TRH só com estrogénios, mesmo se tomada a longo prazo
- com a utilização anterior de TRH combinada tomada a curto prazo
Risco de cancro da mama se existir uma história familiar de cancro da mama (11)
- Um estudo de modelização realizado no Reino Unido em 2024 concluiu que, para uma mulher com um historial familiar "médio" que não toma MHT, o risco cumulativo de cancro da mama (entre os 50 e os 80 anos) é de 9,8% e o risco de morte por cancro da mama é de 1,7%.
- neste modelo, calculou-se que 5 anos de exposição a MHT de ciclo combinado (idade 50-55 anos) aumentam estes riscos para 11,0% e 1,8%, respetivamente.
- Para uma mulher com uma história familiar "forte" que não toma MHT, o risco cumulativo de cancro da mama é de 19,6% (idade 50-80 anos) e o risco de morrer de cancro da mama é de 3,2%. Com 5 anos de exposição à MHT (idade 50-55 anos), este modelo mostrou que estes riscos aumentam para 22,4% e 3,5%, respetivamente. (11)
- por exemplo, para uma mulher "média" de 51 anos de idade que toma TRH combinada durante 5 anos, a probabilidade de desenvolver cancro da mama atribuível à TRH é de 1 em 67
- para as pessoas com um forte historial familiar, a probabilidade respectiva é de 1 em 30
- os autores concluem que, embora as pessoas com uma história familiar significativa ("forte") de cancro da mama tenham um risco de base substancialmente aumentado de desenvolver cancro da mama, a maior parte da incidência e mortalidade por cancro da mama neste grupo será atribuível ao seu risco de base e não à adição de TRH tomada aos 50 anos
- por exemplo, para uma mulher "média" de 51 anos de idade que toma TRH combinada durante 5 anos, a probabilidade de desenvolver cancro da mama atribuível à TRH é de 1 em 67
Nota:
Qualquer risco de cancro da mama deve ser considerado no contexto dos benefícios e riscos globais associados à toma de terapêutica hormonal na menopausa (MHT), incluindo o controlo dos sintomas da menopausa, a melhoria da qualidade de vida e o impacto a longo prazo na saúde óssea e cardiovascular. A decisão de tomar MHT, a dose de MHT e a duração da sua utilização devem ser tomadas numa base individualizada, após discussão dos benefícios e riscos com as mulheres, para as ajudar a fazer uma escolha informada sobre a sua saúde e cuidados.
Referência:
- Collaborative Group on Hormonal Factors for Breast Cancer (Grupo colaborativo sobre factores hormonais para o cancro da mama). Breast cancer and hormone replacement therapy (Cancro da mama e terapia de substituição hormonal): Collaborative reanalysis from 51 individual epidemiological studies. Lancet 1997; 350: 1047-1060
- Grupo de redação para os investigadores da Iniciativa para a Saúde das Mulheres. Risks and benefits of estrogen plus progestin in healthy postmenopausal women. JAMA 2002; 288: 321- 333
- Anderson GL, Limacher M, Assaf AR et al; Comité de Direção da Iniciativa para a Saúde das Mulheres. Effects of conjugated equine estrogen in postmenopausal women with hysterectomy: The Women's Health Initiative randomized controlled trial. JAMA, 2004; 291: 1701-12
- Million Women Study Collaborators. Breast cancer and hormone-replacement therapy in the Million Women Study (Cancro da mama e terapia de substituição hormonal no estudo Milhões de Mulheres). Lancet 2003; 362: 419-427
- Gigerenzer G. How innumeracy can be exploited, In Reckoning with Risk, publishers Penguin Group, 2003
- National Institute for Health and Care Excellence; Menopause; Clinical Guideline - methods, evidence and recommendations (NG23), 2015 www.nice.org.uk/guidance/ ng23
- Grupo de Colaboração sobre Factores Hormonais para o Cancro da Mama. Type and timing of menopausal hormone therapy and breast cancer risk: individual participant meta-analysis of the worldwide epidemiological evidence, doi.org/10.1016/S0140- 6736(19)31709-X
- Chlebowski RT, Anderson GL, Aragaki AK et al. Associação da terapia de substituição hormonal na menopausa com a incidência e a mortalidade por cancro da mama durante o acompanhamento a longo prazo dos ensaios clínicos aleatórios da Iniciativa para a Saúde da Mulher. JAMA, 2020; 324: 369-380.
- MHRA (agosto de 2019). Terapia de substituição hormonal e risco de cancro da mama
- Vinogradova Y, Coupland C, Hippisley-Cox J. Uso de terapia de reposição hormonal e risco de câncer de mama: estudos de caso-controle aninhados usando os bancos de dados QResearch e CPRD. BMJ 2020;371:m3873.
- Huntley C et al. Breast cancer risk assessment for prescription of Menopausal Hormone Therapy in women who have a family history of breast cancer (Avaliação do risco de cancro da mama para prescrição de terapia hormonal na menopausa em mulheres com antecedentes familiares de cancro da mama). Jornal Britânico de Clínica Geral 9 de maio de 2024.
Páginas relacionadas
- Terapia de substituição hormonal (HRT) em doentes com cancro da mama
- Cancro da mama
- Terapia de substituição hormonal
- Tibolona
- Doenças cardíacas e TRH
- Risco de cancro se parar a TRH
- Indicações clínicas para a TRH (terapia de substituição hormonal)
- Orientações da NICE - HRT e risco de cancro da mama
- Revisão das provas sobre o risco de cancro da mama e a TRH
Crie uma conta para adicionar anotações à página
Adicione informações a esta página que seriam úteis de ter à mão durante uma consulta, como um endereço web ou número de telefone. Estas informações serão sempre apresentadas quando visitar esta página